Sequencing and Analysis of Mitochondrial Genome of Chouioia cunea
-
摘要:
本文通过Illumina二代测序技术对周氏啮小蜂Chouioia cunea线粒体基因组进行测序、组装和注释,并分析其结构特点和碱基组成;使用最大似然法重建系统发育树,分析姬小蜂科Eulophidae内的系统发育关系。结果表明,周氏啮小蜂线粒体基因组序列全长14 704 bp,包含 13个蛋白质编码基因、22个tRNA基因和2个rRNA基因。基因组全序列的AT含量为85.0%,表现出明显的AT偏向性。13个蛋白质编码基因均以典型的ATN为起始密码子,以TAA为终止密码子。除trnS1和trnP基因外,其余20个tRNAs 的二级结构均为典型的三叶草结构,二级结构中有U-U碱基错配现象。系统发育分析显示,姬小蜂科的所有物种聚在同一分支,支持该科的单系性;周氏啮小蜂与亮腹釉小蜂Tamarixia radiata聚为一支,在系统发育树上关系最近。本研究在线粒体基因组水平探讨周氏啮小蜂的线粒体基因组结构特征,分析其在姬小蜂科内的分类地位,为揭示姬小蜂科昆虫的系统发育和进化关系提供理论依据。
Abstract:Chouioia cunea belongs to the family Eulophidae and is an important endoparasitic natural enemy of the pupal stage of Hyphantria cunea. It possesses a high parasitism rate and strong fecundity. In this paper, the mitochondrial genome of Chouioia cunea was sequenced, assembled, and annotated using Illumina next-generation sequencing technology, and its structural characteristics and base composition were analyzed. The maximum likelihood method was employed to reconstruct the phylogenetic tree and analyze the phylogenetic relationships within Eulophidae. The results showed that the mitochondrial genome sequence of Chouioia cunea was 14,704 bp in length, including 13 protein-coding genes, 22 tRNA genes, and 2 rRNA genes. The AT content of the whole genome sequence was 85.0%, indicating a significant AT bias. All 13 protein-coding genes have the typical ATN as the start codon and TAA as the stop codon. Except for the trnS1 and trnP genes, the secondary structures of the other 20 tRNAs exhibited a typical cloverleaf structure, and a U-U base mismatch was found in the secondary structure. Phylogenetic analysis indicated that all species of Eulophidae formed a single clade, supporting the monophyly of the family. Chouioia cunea is closely related to Tamarixia radiata in the phylogenetic tree. In this study, the mitochondrial genome structure and taxonomic status of Chouioia cunea were analyzed at the mitochondrial genome level, providing a theoretical basis for understanding the phylogenetic and evolutionary relationships of Eulophidae.
-
昆虫线粒体基因是指存在于昆虫细胞线粒体中的遗传物质,线粒体基因组相对较小,大小为(14~20 kb)[1],由一圈环状DNA组成。昆虫线粒体基因组包含蛋白质编码基因(PCGs)、转运RNA基因(tRNA)和核糖体RNA基因(rRNA)等。其中,蛋白质编码基因数量相对较少,一般为13个,其主要功能为编码线粒体内的蛋白质。昆虫线粒体基因组的特点是具有高度保守性和紧凑性。相比于其他真核生物的线粒体基因组,昆虫线粒体基因组的基因密度较高,基因之间往往没有非编码序列[2],此外,昆虫线粒体基因组的遗传方式为单亲遗传。昆虫线粒体基因组在昆虫分类学、进化研究和种群遗传学等领域具有重要的应用价值,还可以作为昆虫物种鉴定和系统发育重建的重要工具[3]。对昆虫线粒体基因组的分析,可以揭示昆虫的亲缘关系、种群结构和遗传多样性等信息。
周氏啮小蜂Chouioia cunea又名白蛾周氏啮小蜂,隶属姬小蜂科Eulophidae周氏啮小蜂属Chouioia的一种昆虫,是一种优势寄生蜂,具有寄生率高、繁殖力强的优点。周氏啮小蜂是美国白蛾Hyphantria cunea蛹期的重要内寄生性天敌,同时还寄生于榆毒蛾 Ivela ochropoda 和柳毒蛾Stilprotia salicis等鳞翅目Lepidoptera害虫的蛹中。周氏啮小蜂能将产卵器刺入美国白蛾等害虫蛹内,并在蛹内发育成长,吸尽寄生蛹中全部营养,素有“森林小卫士”之美誉[4]。
线粒体全基因组已成为膜翅目Hymenoptera昆虫分子系统学研究的重要分子标记之一,并广泛应用于膜翅目昆虫各个阶元的研究中。本研究利用Illumina测序平台完成周氏啮小蜂的线粒体基因组测序,对基因组序列进行拼装和注释,分析线粒体基因组序列特征,以期丰富基因组学的基础数据,同时基于13个蛋白质编码基因(PCGs)序列,采用最大似然法(Maximum likelihood,ML)构建系统发育进化树,为揭示姬小蜂科昆虫的分类地位及起源进化关系提供理论依据。
1. 材料与方法
1.1 供试昆虫采集与保存
周氏啮小蜂成虫于2022年采集于北京市。标本用99%酒精浸泡,置于−20 ℃保存备用。
1.2 DNA提取与基因组测序
采用十六烷基三甲基溴化铵(CTAB)方法从成虫腿中提取总基因组DNA。1 mg的DNA用于制备DNA文库。随后,在Illumina NovaSeq 6000平台上,使用150 bp的配对reads对DNA文库进行测序。FastQC用于检查数据的质量。质量控制标准如下:去除reads中的adapter序列,剪切去除5'端含有非A、T、C、G的碱基;修剪测序质量较低的reads末端(测序质量值小于Q20);去除含N 的比例达10%的reads;弃去adapter及质量修剪后长度小于75 bp的小片段,得到高质量数据。
1.3 线粒体基因组拼接与注释
使用Novoplasty v 2.7组装线粒体基因组[5]。覆盖的深度由Geneious软件来确定[6]。利用MITOS 网页服务器[7]和MitoZ v3.0[8]对线粒体基因组进行注释。MitoZ是一种能够快速地从二代原始测序数据中“一键式”地得到完成注释及可视化的线粒体基因组的工具。输入原始下机数据,MitoZ使用同源预测的方法对线粒体蛋白基因进行注释,直接输出已完成注释的线粒体基因组(Genbank格式)和可视化结果。本文数据注释得到的结果包含13个蛋白质编码基因(PCGs)、22个tRNA基因和2个rRNA基因(rrnL和rrnS)。利用CGView软件(http:// stothard.afns.ualberta.ca/cgview_server/)对周氏啮小蜂线粒体基因组进行圈图绘制[9]。
1.4 线粒体基因组碱基组成分析
使用Geneious 软件统计核苷酸的碱基组成,包括AT含量、AT偏斜和GC偏斜等,利用Geneious 软件与MEGA软件进行PCGs的氨基酸使用情况分析。通过MITOS 网页服务器对周氏啮小蜂线粒体基因组中tRNA基因的二级结构模型进行预测。基于预测结果,利用Adobe Illustrator绘制tRNA的二级结构。
1.5 系统发育进化分析
基于姬小蜂科4个种昆虫(表1)13个PCGs序列,以金小蜂科Pteromalidae的蚜虫楔缘金小蜂Pachyneuron aphidis和大肠缘金小蜂Muscidifurax similadanacus作为外群,利用MEGA软件进行序列比对,分别基于ML法和BI法重建系统发育树,采用Bootstrap(
1000 次重复)检验ML树各分支节点的置信值[10]。表 1 用于线粒体基因组分析的昆虫物种信息Table 1. Information of the insect species for phylogenetic analysis in mitochondrial genome科名 物种 GenBank登录号 姬小蜂科
Eulophidae潜叶蛾伲姬小蜂Necremnus tutae MT916846 霍氏啮小蜂Tetrastichus howardi MZ334468 亮腹釉小蜂Tamarixia radiata MN123622 周氏啮小蜂Chouioia cunea MW192646 周氏啮小蜂Chouioia cunea 本研究新测定 金小蜂科
Pteromalidae大肠缘金小蜂Muscidifurax similadanacus MT712139 丽蝇蛹集金小蜂Nasonia vitripennis MT712141 2. 结果与分析
2.1 周氏啮小蜂线粒体基因组的序列与结构
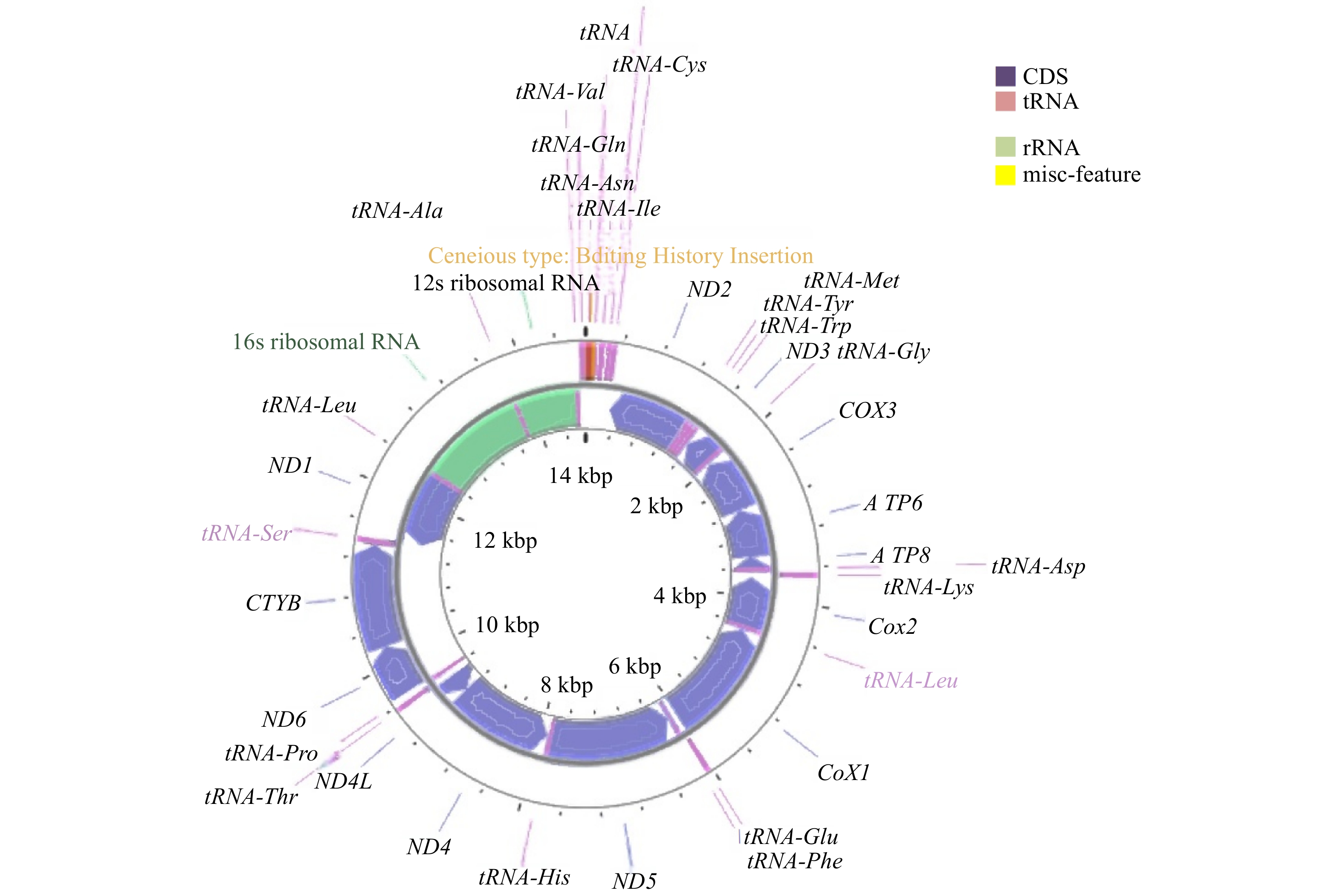
周氏啮小蜂线粒体基因组一共有37个基因(GenBank登录号PP776024),全长14 704 bp,呈双链闭合环状结构,包含13个蛋白质编码基因(PCGs)、22个tRNA基因和2个rRNA基因(rrnL和rrnS)。周氏啮小蜂线粒体基因组基因之间存在重叠或基因间隔区。在不同的位置有27个基因间隔区,最长的为12 bp,在nad4l与trnT基因之间;有9处基因重叠区,最长的为7 bp,在atp8与atp6基因以及nad4l与nad4基因之间(图1和表2)。
表 2 周氏啮小蜂线粒体基因组组成Table 2. Composition of the mitochondrial genome of Chouioia cunea基因 方向 起始位置/bp 终止位置/bp 基因长度/bp 基因间隔/bp 起始密码子 终止密码子 反密码子 trnN F 1 67 67 − AAC trnS1 F 68 126 59 0 TAG trnI F 134 202 69 7 ATC trnR F 213 266 54 10 CGA trnC F 269 331 63 2 TGC nad2 R 331 1 347 1 017 −1 ATT TAA trnY R 1 354 1 419 66 6 TAC trnW R 1 420 1 486 67 0 TGA trnM R 1 488 1 551 64 1 ATC nad3 R 1 552 1 902 351 0 ATA TAA trnG R 1 903 1 967 65 0 GGA cox3 R 1 974 2 759 786 6 ATG TAA atp6 R 2 759 3 433 675 −1 ATG TAA atp8 R 3 427 3 585 159 −7 ATT TAA trnD R 3 586 3 651 66 0 GAC trnK F 3 653 3 721 69 1 AAA cox2 R 3 724 4 404 681 2 ATA TAA trnL2 R 4 405 4 469 65 0 TTA cox1 R 4 472 6 004 1 533 2 ATG TAA trnE F 6 012 6 079 68 7 GAA trnF R 6 081 6 144 64 1 TTC nad5 R 6 145 7 825 1 681 0 ATT TAA trnH R 7 826 7 891 66 0 CAC nad4 R 7 896 9 233 1 338 4 ATG TAA nad4l R 9 227 9 514 288 −7 ATA TAA trnT F 9 527 9 593 67 12 ACA trnP R 9 593 9 659 67 −1 CCA nad6 F 9 660 10 217 558 0 ATT TAA cob R 10 217 11 359 1 143 −1 ATG TAA trnS2 F 11 358 11 424 67 −2 TCA nad1 R 11 423 12 358 936 −2 ATA TAA trnL1 R 12 359 12 426 68 0 CTA rrnL R 12 427 13 757 1 331 0 trnA R 13 758 13 821 64 0 GCA rrnS R 13 822 14 571 750 0 trnV R 14 572 14 636 65 0 GTA trnQ F 14 636 14 701 66 −1 CAA 注:基因间隔列正数表示间隔长度,负数表示重叠长度。 2.2 线粒体基因组核苷酸组成
周氏啮小蜂线粒体基因组的核苷酸组成表现出明显的A和T偏向性。全基因组AT含量为85.0%,其中A的含量为45.0%,T的含量为85.0%,G的含量为6.8%,C的含量为8.2%。其中,tRNA 的AT含量为88.3%,rRNA的AT含量为88.2%,PCGs的AT含量范围在76.6%(cox1)~94.4%(atp8)(表3)。
表 3 周氏啮小蜂线粒体基因组核苷酸组成Table 3. Nucleotide composition of Chouioia cunea mitochondrial genome区域 T含量/% C含量/% A含量/% G含量/% AT含量/% AT-skew GC-skew 全序列 40.0 8.2 45.0 6.8 85.0 0.059 −0.093 tRNAs 44.2 6.1 44.1 5.5 88.3 −0.001 −0.050 rRNAs 46.0 7.3 42.2 4.6 88.2 −0.043 −0.227 atp6 36.6 8.3 46.7 8.4 83.3 0.121 0.006 atp8 40.9 1.9 53.5 3.8 94.4 0.133 0.333 cob 45.9 10.2 33.7 10.1 79.6 −0.153 −0.005 cox1 32.5 12.8 44.1 10.7 76.6 0.151 −0.089 cox2 36.7 11.3 43.8 8.2 80.5 0.088 −0.159 cox3 32.6 11.7 46.6 9.2 79.2 0.177 −0.120 nad1 38.2 9.7 44.9 7.2 83.1 0.081 −0.148 nad2 40.4 3.5 51.5 4.5 91.9 0.121 0.125 nad3 36.2 8.0 49.6 6.3 85.8 0.156 −0.119 nad4 37.7 7.7 48.7 5.9 86.4 0.127 −0.132 nad4l 39.6 7.3 50.7 2.4 90.7 0.123 −0.505 nad5 38.9 7.5 47.5 6.1 86.4 0.100 −0.103 nad6 47.2 5.2 43.6 3.9 90.8 −0.040 −0.143 注:AT-skew =(A的个数−T的个数)/(A的个数+T的个数),GC-skew =(G的个数−C的个数)/(G的个数+C的个数)。 周氏啮小蜂核苷酸链的偏斜统计(AT-skew=0.059,GC-skew=−0.093)表明核苷酸链中A的含量大于T的含量,C的含量大于G的含量。周氏啮小蜂线粒体基因组中的13个PCGs的偏斜统计显示,除cob基因(AT-skew=−0.153)和nad6基因(AT-skew=−0.040)外,其余11个基因的AT-skew均为正值(0.081~0.177)。除atp6基因(GC-skew=0.006)和atp8基因(GC-skew=0.333)以及nad2基因(GC-skew=0.125)外,其余10个基因的GC-skew均为负值(−0.505~−0.005)。以上结果表明,13个PCGs出现了明显的AT偏向性和较明显的C偏向性。
2.3 PCGs和密码子使用频率
周氏啮小蜂线粒体基因组包含13个PCGs,分别是atp6、atp8、cob、cox1、cox2、cox3、nad1、nad2、nad3、nad4、nad4l、nad5和nad6,总长度为14 017 bp,占全基因组的95.33%。其中,最长的基因是nad5,长度为1 681 bp;最短的基因是atp8,长度为 159 bp。周氏啮小蜂线粒体基因组中的13个PCGs基因均以典型的ATN为起始密码子,以TAA为终止密码子(表2),2个基因(nad6和cob)编码在N链上,其余11个基因编码在J链上(图1)。
周氏啮小蜂线粒体蛋白编码基因相对密码子使用频率最高的是TTA(n=422,RSCU为3.60),使用频率最低的是GCG(n=1,RSCU为0.13)。平均使用频率最高的3个氨基酸分别是异亮氨酸(Ile,17.20%)、亮氨酸(Leu,14.36%)和天冬氨酸(Asn,11.10%),使用频率最低的3个氨基酸分别是色氨酸(Trp,0.37%)、丙氨酸(Ala,0.65%)和甘氨酸(Gly,0.75%)(表4)。
表 4 周氏啮小蜂线粒体基因组相对密码子使用频率Table 4. Relative synonymous codon usage(RSCU)of Chouioia cunea mitochondrial genome氨基酸 密码子 数量/个 RSCU 氨基酸 密码子 数量/个 RSCU 丙氨酸 Ala GCG 1 0.13 脯氨酸 Pro CCG 2 0.15 GCA 13 1.63 CCA 20 1.54 GCC 8 1.00 CCT 18 1.38 GCT 10 1.25 CCC 12 0.92 半胱氨酸 Cys TGT 28 1.47 谷氨酰胺 Gln CAG 26 0.53 TGC 10 0.53 CAA 72 1.47 天冬氨酸 Asp GAT 50 1.61 精氨酸 Arg CGG 5 0.91 GAC 12 0.39 CGA 7 1.27 谷氨酸 Glu GAG 17 0.40 CGT 6 1.09 GAA 69 1.60 CGC 4 0.73 苯丙氨酸 Phe TTT 285 1.47 AGG 29 1.00 TTC 102 0.53 AGA 43 1.48 甘氨酸 Gly GGG 8 0.86 丝氨酸 Ser AGT 35 1.2 GGA 12 1.30 AGC 12 0.41 GGT 14 1.51 TCG 9 0.31 GGC 3 0.32 TCA 43 1.48 组氨酸 His CAT 52 1.63 TCT 40 1.37 CAC 12 0.38 TCC 22 0.76 异亮氨酸 Ile ATT 358 1.58 苏氨酸 Thr ACG 6 0.22 ATA 389 1.81 ACA 42 1.57 ATC 96 0.42 ACT 34 1.27 赖氨酸 Lys AAG 64 0.25 缬氨酸 Val ACC 25 0.93 AAA 448 1.75 GTG 8 0.37 天冬氨酸 Asn AAT 494 1.82 GTA 40 1.86 AAC 50 0.18 GTT 27 1.26 亮氨酸 Leu CTA 91 0.78 色氨酸 Trp GTC 11 0.51 CTT 52 0.44 酪氨酸 Tyr TGG 18 0.54 CTC 24 0.20 TAC 43 1.48 TTA 422 3.60 TAT 321 1.67 TTG 82 0.70 CTG 33 0.28 甲硫氨酸 Met ATG 41 0.19 2.4 RNA基因的结构
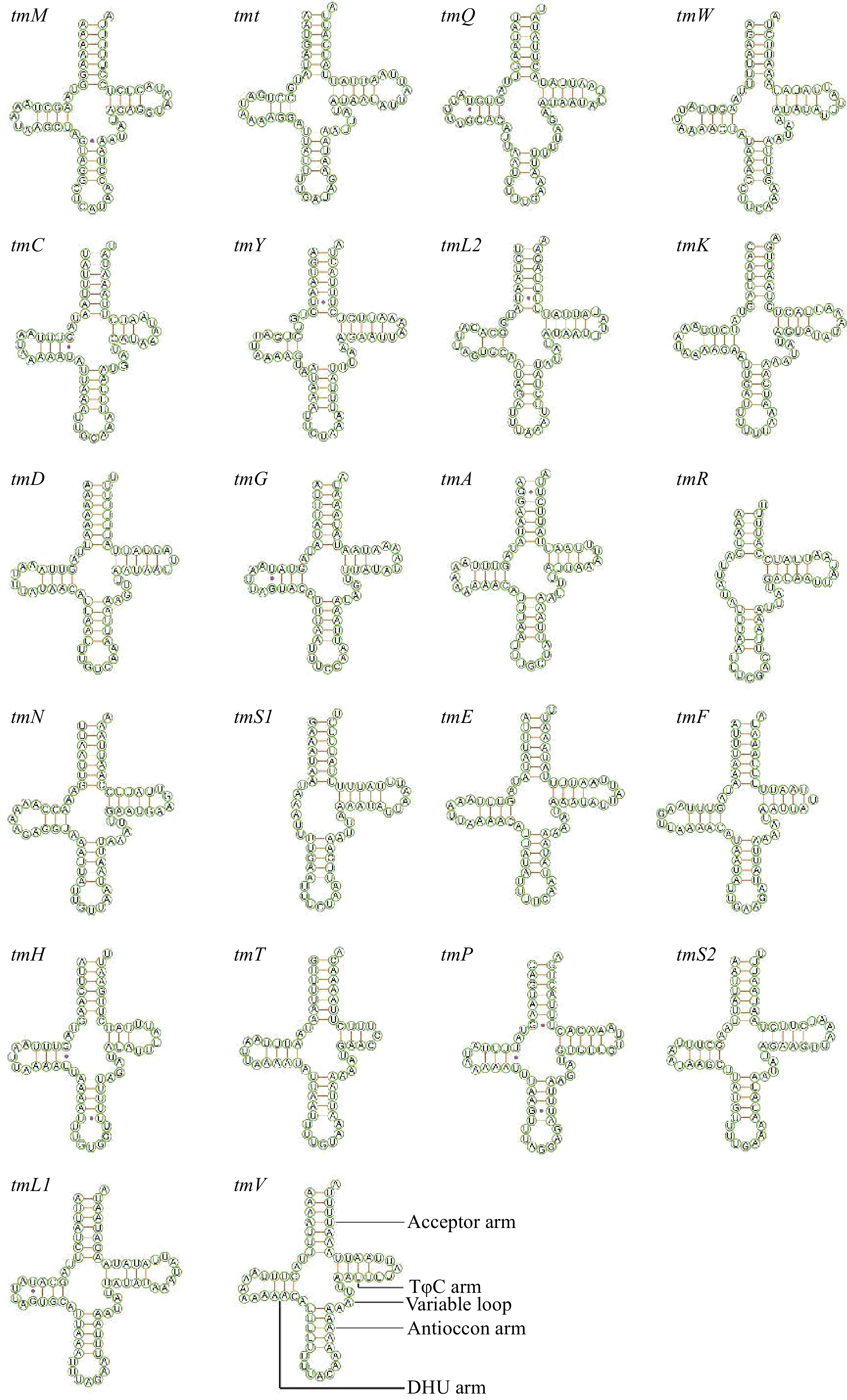
周氏啮小蜂线粒体基因组中,有22个tRNA基因 ,分别为trnA、trnC、trnD、trnE、trnF、trnG、trnH、trnI、trnK、trnL1、trnL2、trnM、trnN、trnP、trnQ、trnR、trnS1、trnS2、trnT、trnV、trnW 和 trnY基因,总长度为1 490 bp,其中最长的基因为trnI和trnK(69 bp),最短的基因为trnR(54 bp)。22个tRNA基因中,10个基因(trnN、trnS1、trnI、trnR、trnC、trnK、trnE、trnT、trnS2和trnQ)编码在N链上,12个基因编码在J链上(图1和表2)。除trnS1和trnR基因缺少DHU臂和DHU环外,其余20个tRNA基因均呈现典型的三叶草二级结构,但trnF和trnM基因具有一个不正常的T环。tRNA 的二级结构中氨基酸接受臂的碱基对大小为7 bp(trnR基因为5 bp),反密码子臂的碱基对为5 bp(trnQ基因反密码子臂的碱基对为3 bp),反密码子环的碱基对为7 bp,TφC臂的大小为3~5 bp,TφC环的大小为1~9 bp,DHU臂的长度为2~4 bp,DHU环的长度为4~ 7 bp。tRNA基因二级结构中存在U-U碱基错配现象(图2)。
两个rRNA基因rrnL和rrnS均位于J链上,其中rrnL基因长度为1 331 bp,位于trnL1基因与trnA基因之间;rrnS基因长度为750 bp,位于trnA基因与trnV基因之间(图1)。 rrnL基因中AT含量为87.3%,rrnS基因中AT含量为89.6%;AT-skew均为负值(分别为−0.029和−0.069),CG-skew均为正值(分别为0.213和0.250),即2个基因中T和C的比例分别高于A和G的比例,且表现出对T的明显偏向性。
2.5 系统发育进化分析
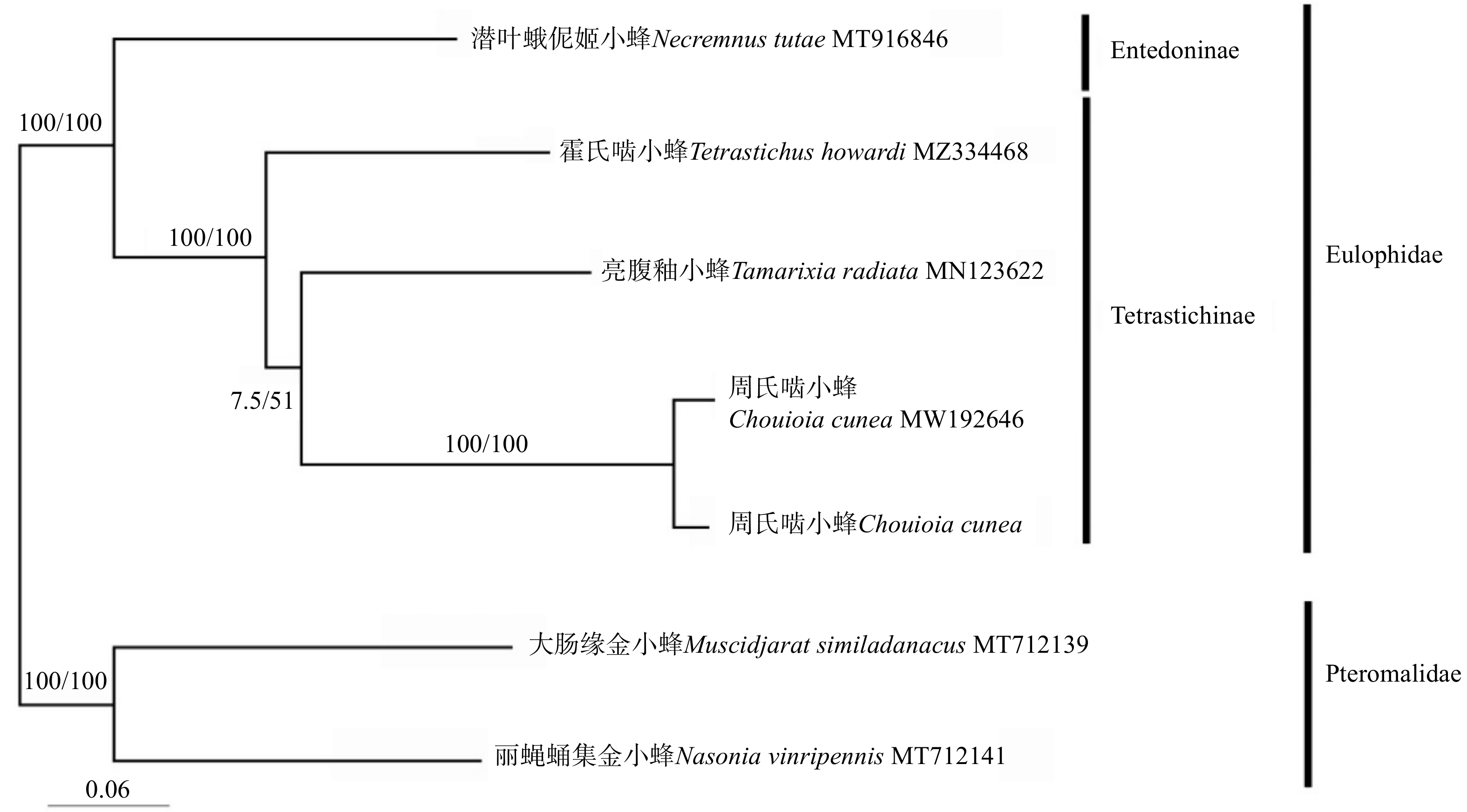
基于本试验所测的周氏啮小蜂及从NCBI数据库中下载的4个姬小蜂科昆虫的线粒体PCGs 数据(表1),以金小蜂科的两个物种作为外群,重建了最大似然法ML树和贝叶斯推论法BI树。结果(图3)显示,2种不同方法重建的系统发育树的拓扑结构一致,姬小蜂科的所有物种聚在同一分支,潜叶蛾伲姬小蜂Necremnus tutae从该分支中最早分出;霍氏啮小蜂和亮腹釉小蜂以及周氏啮小蜂所在分支的自举值和后验概率分别为100和1,其中亮腹釉小蜂和周氏啮小蜂的亲缘关系相较于霍氏啮小蜂更近。
3. 结论与讨论
线粒体广泛存在于昆虫体内,其在控制昆虫的新陈代谢、生命周期及凋亡等方面发挥着重要作用。本研究主要通过对周氏啮小蜂线粒体基因组的测序、注释、特征分析以及系统发育树的构建,明确了周氏啮小蜂的线粒体基因组结构特征及其与数据库中其他姬小蜂科昆虫的系统发育关系。周氏啮小蜂线粒体基因组的结构、核苷酸组成、密码子使用频率、rRNA基因、 tRNA基因二级结构、控制区的组成等与已发表的小蜂总科线粒体基因组结构及组成基本一致[11-15]。周氏啮小蜂的线粒体基因组长14 704 bp,AT含量为85.0%,基因组的AT含量较高,同已报道的小蜂总科其他昆虫的线粒体基因排列一致[16]。周氏啮小蜂线粒体基因组基因之间也存在重叠或基因间隔区,姬小蜂科昆虫线粒体基因组基因之间的重叠或间隔一般较短[17]。此研究结果表明周氏啮小蜂线粒体基因组中基因间隔区最长的为12 bp,与前人研究结果基本一致[18]。周氏啮小蜂线粒体基因组的核苷酸组成存在明显的偏向性,AT含量明显高于GC 含量,表现出明显的AT 碱基偏斜,符合昆虫体内线粒体基因AT 比例高的特点[19]。
周氏啮小蜂线粒体基因组中,除trnS1和trnR基因缺少DHU臂和DHU环外,其余20个tRNA基因均呈现典型的三叶草二级结构,但trnF和trnM基因具有一个不正常的T环。在许多昆虫的线粒体基因组中,缺乏DHU臂和DHU环是一种正常现象[20]。
周氏啮小蜂线粒体基因组中的13个PCGs基因均以典型的ATN为起始密码子,以TAA为终止密码子。PCGs 中平均使用频率最高的3个氨基酸分别是异亮氨酸、亮氨酸和天冬氨酸,使用频率最低的3个氨基酸是色氨酸、丙氨酸和甘氨酸,这与前人研究结果基本一致[21]。
本研究中系统发育树结果显示姬小蜂科为单系群,潜叶蛾伲姬小蜂从该分支中最早分化而出。霍氏啮小蜂和亮腹釉小蜂以及周氏啮小蜂均以高的支持率聚为一支,与前人研究结果相近[22]。本研究结果为周氏啮小蜂的群体遗传学和分子生态学研究提供了基础信息,丰富了姬小蜂科线粒体基因组的序列、结构及组成信息,为后续姬小蜂科昆虫的系统发育和进化研究提供了参考。
致谢:本研究得到国家自然科学基金项目(32100355, 32100352)和安徽师范大学大学生创新创业训练计划项目资助,谨致谢忱!
-
表 1 用于线粒体基因组分析的昆虫物种信息
Table 1 Information of the insect species for phylogenetic analysis in mitochondrial genome
科名 物种 GenBank登录号 姬小蜂科
Eulophidae潜叶蛾伲姬小蜂Necremnus tutae MT916846 霍氏啮小蜂Tetrastichus howardi MZ334468 亮腹釉小蜂Tamarixia radiata MN123622 周氏啮小蜂Chouioia cunea MW192646 周氏啮小蜂Chouioia cunea 本研究新测定 金小蜂科
Pteromalidae大肠缘金小蜂Muscidifurax similadanacus MT712139 丽蝇蛹集金小蜂Nasonia vitripennis MT712141 表 2 周氏啮小蜂线粒体基因组组成
Table 2 Composition of the mitochondrial genome of Chouioia cunea
基因 方向 起始位置/bp 终止位置/bp 基因长度/bp 基因间隔/bp 起始密码子 终止密码子 反密码子 trnN F 1 67 67 − AAC trnS1 F 68 126 59 0 TAG trnI F 134 202 69 7 ATC trnR F 213 266 54 10 CGA trnC F 269 331 63 2 TGC nad2 R 331 1 347 1 017 −1 ATT TAA trnY R 1 354 1 419 66 6 TAC trnW R 1 420 1 486 67 0 TGA trnM R 1 488 1 551 64 1 ATC nad3 R 1 552 1 902 351 0 ATA TAA trnG R 1 903 1 967 65 0 GGA cox3 R 1 974 2 759 786 6 ATG TAA atp6 R 2 759 3 433 675 −1 ATG TAA atp8 R 3 427 3 585 159 −7 ATT TAA trnD R 3 586 3 651 66 0 GAC trnK F 3 653 3 721 69 1 AAA cox2 R 3 724 4 404 681 2 ATA TAA trnL2 R 4 405 4 469 65 0 TTA cox1 R 4 472 6 004 1 533 2 ATG TAA trnE F 6 012 6 079 68 7 GAA trnF R 6 081 6 144 64 1 TTC nad5 R 6 145 7 825 1 681 0 ATT TAA trnH R 7 826 7 891 66 0 CAC nad4 R 7 896 9 233 1 338 4 ATG TAA nad4l R 9 227 9 514 288 −7 ATA TAA trnT F 9 527 9 593 67 12 ACA trnP R 9 593 9 659 67 −1 CCA nad6 F 9 660 10 217 558 0 ATT TAA cob R 10 217 11 359 1 143 −1 ATG TAA trnS2 F 11 358 11 424 67 −2 TCA nad1 R 11 423 12 358 936 −2 ATA TAA trnL1 R 12 359 12 426 68 0 CTA rrnL R 12 427 13 757 1 331 0 trnA R 13 758 13 821 64 0 GCA rrnS R 13 822 14 571 750 0 trnV R 14 572 14 636 65 0 GTA trnQ F 14 636 14 701 66 −1 CAA 注:基因间隔列正数表示间隔长度,负数表示重叠长度。 表 3 周氏啮小蜂线粒体基因组核苷酸组成
Table 3 Nucleotide composition of Chouioia cunea mitochondrial genome
区域 T含量/% C含量/% A含量/% G含量/% AT含量/% AT-skew GC-skew 全序列 40.0 8.2 45.0 6.8 85.0 0.059 −0.093 tRNAs 44.2 6.1 44.1 5.5 88.3 −0.001 −0.050 rRNAs 46.0 7.3 42.2 4.6 88.2 −0.043 −0.227 atp6 36.6 8.3 46.7 8.4 83.3 0.121 0.006 atp8 40.9 1.9 53.5 3.8 94.4 0.133 0.333 cob 45.9 10.2 33.7 10.1 79.6 −0.153 −0.005 cox1 32.5 12.8 44.1 10.7 76.6 0.151 −0.089 cox2 36.7 11.3 43.8 8.2 80.5 0.088 −0.159 cox3 32.6 11.7 46.6 9.2 79.2 0.177 −0.120 nad1 38.2 9.7 44.9 7.2 83.1 0.081 −0.148 nad2 40.4 3.5 51.5 4.5 91.9 0.121 0.125 nad3 36.2 8.0 49.6 6.3 85.8 0.156 −0.119 nad4 37.7 7.7 48.7 5.9 86.4 0.127 −0.132 nad4l 39.6 7.3 50.7 2.4 90.7 0.123 −0.505 nad5 38.9 7.5 47.5 6.1 86.4 0.100 −0.103 nad6 47.2 5.2 43.6 3.9 90.8 −0.040 −0.143 注:AT-skew =(A的个数−T的个数)/(A的个数+T的个数),GC-skew =(G的个数−C的个数)/(G的个数+C的个数)。 表 4 周氏啮小蜂线粒体基因组相对密码子使用频率
Table 4 Relative synonymous codon usage(RSCU)of Chouioia cunea mitochondrial genome
氨基酸 密码子 数量/个 RSCU 氨基酸 密码子 数量/个 RSCU 丙氨酸 Ala GCG 1 0.13 脯氨酸 Pro CCG 2 0.15 GCA 13 1.63 CCA 20 1.54 GCC 8 1.00 CCT 18 1.38 GCT 10 1.25 CCC 12 0.92 半胱氨酸 Cys TGT 28 1.47 谷氨酰胺 Gln CAG 26 0.53 TGC 10 0.53 CAA 72 1.47 天冬氨酸 Asp GAT 50 1.61 精氨酸 Arg CGG 5 0.91 GAC 12 0.39 CGA 7 1.27 谷氨酸 Glu GAG 17 0.40 CGT 6 1.09 GAA 69 1.60 CGC 4 0.73 苯丙氨酸 Phe TTT 285 1.47 AGG 29 1.00 TTC 102 0.53 AGA 43 1.48 甘氨酸 Gly GGG 8 0.86 丝氨酸 Ser AGT 35 1.2 GGA 12 1.30 AGC 12 0.41 GGT 14 1.51 TCG 9 0.31 GGC 3 0.32 TCA 43 1.48 组氨酸 His CAT 52 1.63 TCT 40 1.37 CAC 12 0.38 TCC 22 0.76 异亮氨酸 Ile ATT 358 1.58 苏氨酸 Thr ACG 6 0.22 ATA 389 1.81 ACA 42 1.57 ATC 96 0.42 ACT 34 1.27 赖氨酸 Lys AAG 64 0.25 缬氨酸 Val ACC 25 0.93 AAA 448 1.75 GTG 8 0.37 天冬氨酸 Asn AAT 494 1.82 GTA 40 1.86 AAC 50 0.18 GTT 27 1.26 亮氨酸 Leu CTA 91 0.78 色氨酸 Trp GTC 11 0.51 CTT 52 0.44 酪氨酸 Tyr TGG 18 0.54 CTC 24 0.20 TAC 43 1.48 TTA 422 3.60 TAT 321 1.67 TTG 82 0.70 CTG 33 0.28 甲硫氨酸 Met ATG 41 0.19 -
[1] 宋凡. 昆虫纲关键类群的比较线粒体基因组学及系统发育研究[D]. 北京:中国农业大学,2016. [2] LIU Q N,XIN Z Z,BIAN D D,et al. The first complete mitochondrial genome for the subfamily Limacodidae and implications for the higher phylogeny of Lepidopt era[J]. Scientific Reports,2016,6(1):35878. doi: 10.1038/srep35878
[3] CAO S Y,WU X B,YAN P,et al. Complete nucleotide sequences and gene organization of mitochondrial genome of Bufo gargarizans[J]. Mitochondrion,2016,6(4):186 − 193.
[4] 李路文,吴冉,何长流,等. 利用白蛾周氏啮小蜂防治美国白蛾试验研究[J]. 中国园艺文摘,2016(7):43 − 45. doi: 10.3969/j.issn.1672-0873.2016.07.017 [5] NICOLAS D,PATRICK M,GUILLAUME S. NOVOPlasty:de novo assembly of organelle genomes from whole genome data[J]. Nucleic Acids Res,2016,4(4):gkw955.
[6] BANKEVICH A,NURK S,ANTIPOV D,et al. A new genome assembly algorithm and its applications to single-cell sequencing[J]. Journal of Computational Biology,2012,19(5):455 − 477. doi: 10.1089/cmb.2012.0021
[7] BERNT M,DONATH A,JUHLING F,et al. MITOS:improved de novo metazoan mitochondrial genome annotation[J]. Mol Phylogenet Evol,2013,69(2):313 − 319. doi: 10.1016/j.ympev.2012.08.023
[8] MENG G,LI Y,YANG C,et al. Mitoz:a toolkit for animal mitochondrial genome assembly,annotation and visualization[J]. Nucleic Acids Res,2019,47(11):e63. doi: 10.1093/nar/gkz173
[9] GRANT J R,STOTHARD P. The CGView Server:A comparative genomics tool for circular genomes[J]. Nucleic Acids Research,2008,36(S2):181 − 184.
[10] NGUYEN L T,SCHMIDT H A,VON HAESELER A,et al. IQ-TREE:A fast and effective stochastic algorithm for estimating maximum-likelihood phylogenies[J]. Molecular Biology and Evolution,2015,32(1):268 − 274. doi: 10.1093/molbev/msu300
[11] 聂瑞娥,杨星科. 鞘翅目昆虫线粒体基因组研究进展[J]. 昆虫学报,2014,57(7):860 − 868. [12] 李欣欣,宋南. 瓢甲科线粒体基因组及系统发生研究[J]. 华中昆虫研究,2017,13:137 − 147. [13] KENECHUKWU N A,LI M,AN L,et al. Comparative analysis of the complete mitochondrial genomes for development application[J]. Frontiers in Genetics,2019,9:651. doi: 10.3389/fgene.2018.00651
[14] SONG N,LI X X,YIN X M,et al. The mitochondrial genomes of ladybird beetles and implications for evolution and phylogeny[J]. International Journal of Biological Macromolecules,2020,147:1193 − 1203. doi: 10.1016/j.ijbiomac.2019.10.089
[15] LI X H,SONG N,ZHANG H. Comparative and phylogenomic analyses of mitochondrial genomes in Coccinellidae(Coleoptera:Coccinelloidea)[J]. PeerJ,2021,9:e12169. doi: 10.7717/peerj.12169
[16] CAMERON SL,DOWTON M,CASTRO LR,et al. Mitochondrial genome organization and phylogeny of two vespid wasps[J]. Genome,2008,51:800 − 808. doi: 10.1139/G08-066
[17] 魏书军,陈学新. 昆虫比较线粒体基因组学研究进展[J]. 应用昆虫学报,2011,48(6):1573 − 1585. doi: 10.7679/j.issn.2095-1353.2011.244 [18] WANG J X,ZHOU Y,XIN Z Z,et al. Differences in the evolution of mitochondrial genome between pollinating and non-pollinating fig wasps[J]. Acta Entomol. Sin,2021,64(4):479 − 489.
[19] 黄卫东. 中国小毛瓢虫族的系统发育研究(鞘翅目:瓢虫科)[D]. 广州:华南农业大学,2016 . [20] SUN Z,ZHANG J,WANG R,et al. Progress of insect mitochindrial genome[J]. Journal of Inspection and Quarantine,2010,20(3):69 − 73.
[21] ZHANG Y,SU T J,HE B,et al. Sequencing and characterization of the Megachile sculpturalis (Hymenoptera:Megachilidae) mitochondrial genome[J]. Mitochondrial DNA,2017,28(3):344 − 346. doi: 10.3109/19401736.2015.1122774
[22] XUE T,BAO Q L,HUI L,et al. The mitochondrial genome of a parasitic wasp,Chouioia cunea Yang (Hymenoptera:Chalcidoidea:Eulophidae) and phylogenetic analysis[J]. Mitochondrial DNA Part B,2021,872 − 874.



 下载:
下载: